Plaquetas bajo cero que cierran heridas
Investigadores del IBIOMED y del CAULE desarrollan un nuevo método para curar las úlceras cutáneas crónicas / Reproducen la respuesta molecular normal de los tejidos / Demuestran que este tratamiento es una alternativa real para conseguir una mejoría evidente e incluso la curación completa de estas lesiones

IBIOMED 1
Las heridas producen una pérdida de la integridad cutánea, del epitelio y del tejido conectivo subcutáneo. Es verdad que el cuerpo humano está diseñado para reparar estas lesiones en un tiempo más o menos determinado según diferentes características, como tipo de herida, zona afectada, daño producido, edad, enfermedades previas… Sin embargo, algunas no cicatrizan, convirtiéndose en úlceras crónicas. En ellas la manipulación externa mediante diversas técnicas es fundamental para llevar la reparación a buen fin.
Esta condición implica un problema importante si se tiene en cuenta su incidencia, el deterioro que producen en la calidad de vida de los pacientes y la repercusión económica que supone. Afecta al 1% de la población adulta y al 3,6% de las personas mayores de 65 años, siendo su prevalencia en Estados Unidos entre 600.000 y 1.500.000 de pacientes. Entre sus causas principales se encuentran la enfermedad venosa, la enfermedad arterial y la neuropatía. Del mismo modo, aunque no son tan comunes, también pueden ser factores desencadenantes de úlceras, los trastornos metabólicos (diabetes mellitus), hematológicos, las enfermedades infecciosas y ciertos medicamentos.
Por ello, dado que existen múltiples factores que conducen a esta patología, se requiere un tratamiento multidisciplinar para la evaluación sistemática del paciente, con el fin de determinar la patogenia, el diagnóstico definitivo y escoger el tratamiento óptimo. Es por esto por lo que el tratamiento de las úlceras crónicas no es tan fácil, precisa de diagnóstico correcto y de una actualización continua en el manejo de las mismas.
Un plan de tratamiento ideal para estas personas debe incluir un enfoque temprano estratégico y coordinado, con el objetivo de ofrecer la opción de tratamiento correcto para cada paciente, basado en una evolución de la fisiopatología subyacente. El tratamiento local incluye limpieza, desbridamiento, control de la infección, si existe, y aplicación de diversos agentes tópicos, tanto desde el punto de vista de la medicación como del uso de apósitos. De manera reciente, se han establecido nuevas estrategias terapéuticas que incluyen reemplazamientos de la piel a través de sustitutos biológicos. En este punto es donde el equipo formado por investigadores del Instituto de Biomedicina de León (IBIOMED) y del Complejo Asistencial Universitario de León (CAULE) vieron una oportunidad terapéutica.
¿Qué han conseguido? Reproducir la respuesta molecular normal de los tejidos y demostrar que este tratamiento es una alternativa real para conseguir una mejoría evidente e incluso la curación completa de las lesiones. Para entender cómo surgió esta idea, según explica Julia Vidán Estévez, jefa de Servicio de Transfusión del CAULE, hay que comprender cómo se produce la reparación natural de los tejidos. En términos generales, se reconocen tres fases consecutivas que se solapan entre sí: una fase inflamatoria aguda, una segunda fase de proliferación y reparación y una tercera fase de remodelado. En estas fases intervienen distintas células y señales moleculares con la meta de formar un tejido de granulación y cicatrización de las heridas. Dentro de estas células, las plaquetas ejercen un papel decisivo en el proceso de curación y reparación de la herida tisular; pero esta función reparadora no está relacionada con las plaquetas en sí mismas, sino con los factores de crecimiento liberados de sus gránulos alfa. «Estos factores de crecimiento son elementos que originan señales bioquímicas capaces de modificar las respuestas de las células del organismo. Se encuentran involucrados en el control del crecimiento y en la diferenciación celular».
En esta línea, añade el investigador Jesús Seco Calvo, el odontólogo americano Robert Marx fue quien en 1997 aportó a la bibliografía científica el término plasma rico en plaquetas como el componente sanguíneo concentrado que se caracteriza por poseer una alta concentración de plaquetas (4 a 6 veces sus valores normales) y que se obtiene tras la extracción de sangre del paciente y su posterior centrifugación. Está compuesto de plasma, plaquetas, factores de crecimiento y restos mínimos de leucocitos.
Desde la primera aplicación del plasma rico en plaquetas se han publicado los beneficios de los factores de crecimiento derivados de las plaquetas en reparación y regeneración de tejidos que se han visto plasmados en la gran cantidad de aplicaciones en distintos terrenos de la medicina, como para el tratamiento de heridas quirúrgicas, patologías musculoesqueléticas, quemaduras, reparación de nervios periféricos; algunas de estas aplicaciones con resultados positivos o muy prometedores.
El problema, tal y como sostiene Vidán Estévez, es que una sola aplicación del producto no sirve de mucho. Necesitan aplicar plasma rico en plaquetas a diario. «Esto supondría extracciones de sangre diariamente para obtenerlo con los métodos convencionales. Algo que no sería viable», asegura el investigador.
Ahí surgió la idea de realizar un procedimiento conocido como plaquetoaféresis, en el que tras una donación se obtiene una aféresis de plaquetas, tal como hacen los donantes de plaquetas. «El sistema consiste en colocar una vía venosa en el paciente a través de la cual se hace pasar la sangre a una centrífuga que por gradiente separa los elementos celulares; posteriormente se reinfunde al paciente el plasma y las células que no se van a utilizar, todo ello en un sistema cerrado y estéril para evitar la contaminación. Con este sistema se puede obtener un gran concentrado de plaquetas», detalla.
Primero se requiere una evaluación del paciente en consulta del Servicio de Transfusión anotando y midiendo las lesiones a tratar. Al paciente se le hace una extracción de analítica completa y tras comprobar que no hay alteraciones se prepara la aféresis de plaquetas alogénicas isogrupo ABO de donante único. Más tarde esta aféresis de plaquetas se alícuota en pequeñas muestras de 5-10 mililitros según el tamaño de la herida. Todo el producto alicuotado perfectamente identificado es criopreservado, es decir se guarda en un ultracongelador a -80 grados centígrados, lo que garantiza estabilidad del producto durante al menos seis meses.
¿Cómo se hace la cura? La primera la realizan en el Servicio de Transfusión del Hospital de León, donde se registra el tamaño de la lesión, se verifica que la úlcera no está infectada y se explica al paciente o familiar el procedimiento. Semanalmente, el paciente debe pasar por el Servicio de Transfusión a recoger las dosis (siete alícuotas) que tiene que almacenar en el congelador de su casa hasta el momento de la administración.
Diariamente, y tras descongelarlo en pocos minutos al baño maría, se administra directamente el producto sobre la zona a tratar que debe estar limpia antes de añadir el producto. «Es recomendable hacer el tratamiento cuando el paciente se vaya a acostar para evitar la movilización y la pérdida del producto, consiguiendo un mayor tiempo de contacto del plasma rico en plaquetas con la herida a tratar», apunta la jefa de Servicio de Transfusión del CAULE.
Se procede a la instilación de la jeringa alicuotada descongelada repartiendo bien todo el contenido por la herida y después se tapa con una gasa limpia, que se deja así hasta el día siguiente. Cuanto más tiempo esté en contacto el plasma rico en plaquetas con la lesión a tratar mejor será el resultado. Cada dos-tres semanas se valora de manera presencial la evolución de las lesiones tratadas.
En esta línea, Seco Calvo puntualiza que se trata de reproducir la respuesta molecular normal de los tejidos a las heridas. «Cuando las plaquetas se adhieren a las moléculas expuestas del epitelio lesionado se activan, y esta activación plaquetaria en respuesta al daño tisular y vascular provoca la formación de un tapón plaquetario y un coágulo hemático, cuyas funciones son la consecución de la hemostasia, y la secreción de proteínas biológicamente activas involucradas en el proceso de curación tisular. Estas proteínas, denominadas factores de crecimiento, son secretadas por la estructura plaquetaria».
La liberación de dichos factores de crecimiento en respuesta a la lesión está coordinada con un aumento en la expresión de receptores específicos para estos factores de crecimiento. En todo este proceso intervienen cambios vasculares, celulares y químicos, que van evolucionando en el transcurso de las distintas fases. En el mejor de los casos conducen a la reparación del tejido y, en casos desfavorables, a la degeneración crónica, al tejido cicatricial y a la formación de fibrosis y adherencias. «Con la aplicación de la aféresis de plaquetas alicuotada congelada y después descongelada tratamos de conseguir el mismo efecto provocando esa liberación de los factores de crecimiento, y así conseguir acelerar la reparación y la regeneración tisular de esas úlceras crónicas», subraya el investigador del IBIOMED.
Este trabajo demuestra como la utilización de plaquetas alogénicas isogrupo ABO procedentes del Servicio de Transfusión se puede emplear en la medicina regenerativa por su capacidad de secretar factores de crecimiento y otros materiales bioactivos tras un procedimiento de congelación a -80ºC y posterior descongelación, que permite la desintegración plaquetaria y liberación de los factores de crecimiento derivados de las plaquetas responsables de la cicatrización de las heridas.
JESÚS SECO CALVO / INVESTIGADOR DEL IBIOMED
«Estamos logrando hallazgos relevantes desde diferentes ámbitos de la investigación»
Jesús Seco Calvo, investigador del IBIOMED, asegura que Castilla y León goza de buena salud en investigación e innovación. De hecho, sostiene que se están logrando hallazgos relevantes desde diferentes ámbitos de la investigación, ya sea básica, aplicada, tecnológica, histórica, paleontológica… Además, considera que estos resultados son transferibles a la sociedad, es decir, tienen un alto grado de aplicación para mejorar, en su caso en particular, la salud de las personas.
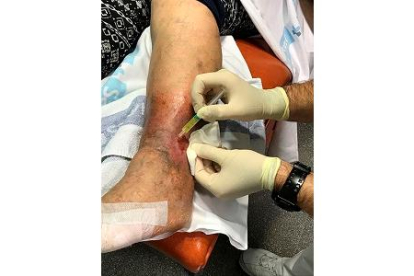
Imagen del tratamiento de una úlcera cutánea crónica.
Sostiene que en la Comunidad se manejan numerosos instrumentos utilizados para el apoyo a la investigación básica, biomédica, entre otros. De igual forma, apunta que cuentan con ayudas para proyectos, con convenios con institutos y centros tecnológicos, con el Instituto de Salud Carlos III…, que fomentan acciones para la contratación, estabilización e intensificación de investigadores. Agradecen todo este apoyo, pero, agrega el investigador del IBIOMED, sería deseable menos burocracia.
A su juicio, la sociedad no premia la innovación y el talento. «No lo hace porque, por una parte, la clase política tiene a la sociedad entretenida, y con la orientación y control de los medios de información, maneja su atención, para que no piense y no reflexione; y por otra, porque bastante premio es poder pagar la factura de la luz. No se entienden las decisiones políticas en este tiempo de pandemia, sin hacer ni caso a los avisos y previsiones de los científicos. Percibo una sociedad callada y adormecida, y una sociedad así es una sociedad sometida», lamenta. En este sentido, Seco Calvo está preocupado por «la manipulación torcidera y partidista del proceso educativo».